Atomun Kuantum Modeli - 1
Bol Bol test çöz ve kendini daima sınava hazır tut.Atomun Kuantum Modeli - 1
11. Sınıf: Kimya - 1. Ünite: Modern Atom teorisi - Atomun Kuantum Modeli Test Soruları
Hatırlatma!
TestSorular'da sadece oturum açmış öğrenciler çözdükleri testlerden puan kazanabilir.
Yok benim amacım puan toplamak değil sadece kendimi geliştirmek istiyorum diyorsan, sorular seni bekliyor.
Hata Bildir!
Bir oyun parkında bulunan çocuklar sürekli hareket hâlindedir. Bir oyuncaktan diğerine giderler ancak bu hareketleri oyun parkının sınırları içindedir. Çocuklar elektrona, oyun parkındaki hareketleri elektronun hareketine benzetilebilir.
Buna göre bu hareket;
I. yörünge,
II. belirli yörünge,
III. orbital
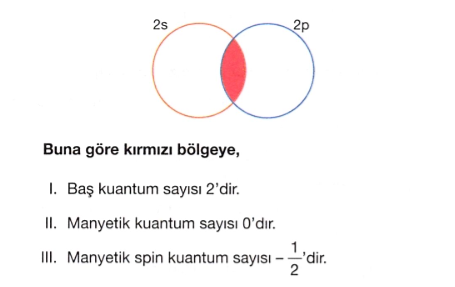
I. Baş - Açısal momentum
II. Açısal momentum - Manyetik
III. Manyetik - Manyetik spin
Bohr Atom Model'inin çok kabul görmemesi ve kısa ömürlü olmasının nedenlerinden biri de ..... .
Bohr Atom Modeli ile ilgili bu cümledeki boş bırakılan yere,
I. sadece tek elektronlu sistemlere uygulanabilmesidir
II. elektronun sadece tanecik özelliği dikkate alınarak oluşturulmasıdır
III. Heisenberg belirsizlik prensibi ile çelişki oluşturmasıdır
Bohr Atom Modeli’nin temelini hidrojen elementinin soğurma ve yayınım spektrumu oluşturur.
Bu spektrumlarda yer alan çizgiler ile ilgili,
I. Elektronların yörüngeler arası geçiş sırasında aldığı ya da verdiği enerjiyi gösterir.
II. Bir element için çizgilerin yeri, soğurma ve yayınım spektrumunda aynıdır.
III. Atomdaki elektron sayısı arttıkça çizgilerin sayısı da artar.
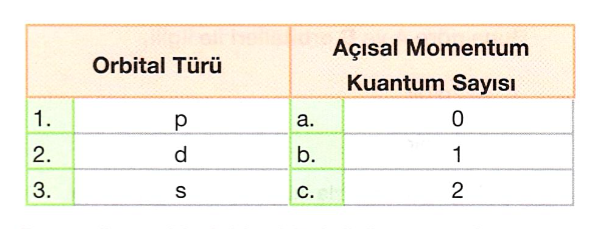
Aşağıda bazı kuantum sayıları verilmiştir.
1. Baş
2. Açısal momentum
3. Manyetik
Bu kuantum sayıları ile ilgili,
I. Sıfır değerini alabilenler 2 ve 3.dür.
II. 2 değerini alabilenler 1 ve 2.dir.
III. 3. + veya - değerde olabilir,
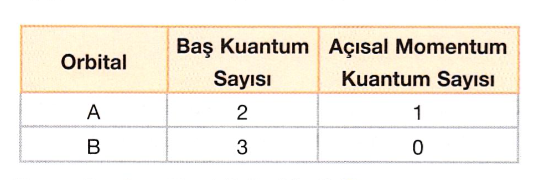
4d alt kabuğundaki orbitallerden biri ile ilgili,
I. Manyetik kuantum sayısı -3 olabilir.
II. Açısal momentum kuantum sayısı 2’dir.
III. Yapısında bir elektron varsa bu elektronun manyetik spin kuantum sayısı net olarak bilinemez.
Çok elektronlu bir atomda 3d orbitalinde yer alan elektron ile ilgili,
I. Baş kuantum sayısı 3’tür.
II. Açısal momentum kuantum sayısı 2’dir.
III. Manyetik kuantum sayısı +2 olabilir.
IV. Manyetik spin kuantum sayısı -1 olabilir,
4. enerji düzeyinde bulunan bir orbitalin x ile belirtilen kuantum sayısı - 2 ’dir.
Buna göre orbital ve x kuantum sayısı ile ilgili,
I. Orbital p olabilir.
II. Orbital f olabilir.
III. x, manyetik kuantum sayısıdır.
IV. Orbitalin baş kuantum sayısı 4’tür.
I. Baş
II. Açısal momentum
III. Manyetik
IV. Manyetik spin